Se você usar este medicamento comum, fale com seu médico agora, a FDA adverte

O que quer que esteja no seu gabinete de remédios, você quer se sentir confiante de que tudo o que está levando é seguro para consumir. Se você usa uma receita diária ou alcance antiácidos após uma grande refeição, confiamos na medicação para ajudar em vez de nos machucar. Agora, um medicamento comum acabou de ser lembrado e você deseja chegar ao seu médico imediatamente se tiver uma das garrafas afetadas. Continue lendo para saber mais sobre o produto da Pfizer que o U.S. A Food and Drug Administration (FDA) alerta pode causar mais mal do que bem.
RELACIONADOS: Estes remédios comuns de azia e dor foram recolhidos, alerta a FDA.
O nome da Pfizer agora é facilmente reconhecido.

Nos últimos anos, Pfizer se tornou um nome familiar. A empresa é reconhecida por ter fabricado a primeira vacina covid-19 do país, ao lado da Biontech, tendo sido originalmente aprovado pelo FDA em DEC. 2020. De acordo com a revisão anual de 2021 da Pfizer, quase 3 bilhões de doses da vacina foram produzidas em 2021 e 4 bilhões são projetados para serem fabricados em 2022.
Antes de fazer manchetes durante a pandemia, no entanto, a Pfizer era amplamente conhecida pelos tratamentos produzidos para outras condições médicas, variando de depressão (na forma de pristiq) a fibromialgia (via lyrica). Agora, a empresa farmacêutica está se lembrando de muitos remédios populares, que é usada para tratar uma condição ainda mais comum.
Cinco lotes de medicação Pfizer foram lembrados.
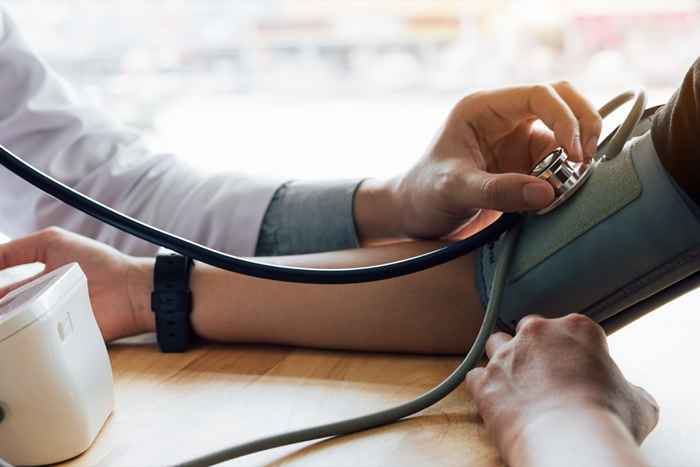
Os Centros de Controle e Prevenção de Doenças (CDC) estima que quase metade dos americanos tem hipertensão, mas apenas cerca de um quarto desses indivíduos têm sua condição sob controle. Accupril é um medicamento frequentemente prescrito para o tratamento da pressão alta, mas alguns desses produtos agora podem representar maiores ameaças à sua saúde.
Em 22 de abril, o FDA anunciou que a Pfizer estava voluntariamente recordando cinco lotes de comprimidos Accupril após o teste encontrou níveis elevados de nitrosamina, ou nnitroso-quinapril, um potencial agente causador de câncer. De acordo com o anúncio da FDA, as nitrosaminas são frequentemente encontradas em água e alimentos, além de carnes curadas e grelhadas, laticínios e legumes. O risco de câncer é aumentado quando as pessoas são expostas a níveis mais altos em longos períodos de tempo. AE0FCC31AE342FD3A1346EBB1F342FCB
Relacionado: Para obter informações mais atualizadas, inscreva-se em nosso boletim informativo diário.
Você deve verificar seu medicamento para ver se faz parte do recall.

Além de tratar a hipertensão, você também pode tomar o Accupril como terapia adjuvante para o gerenciamento de insuficiência cardíaca, quando combinada com diuréticos e/ou digitais (as abordagens de terapia convencional), de acordo com o aviso da FDA. As pessoas que tomam Accupril (também conhecidas por seu nome genérico, Quinapril cloridrato) para qualquer uma dessas condições devem verificar se seus produtos fazem parte do recall.
Em sua garrafa, procure o Código Nacional de Drogas (NDC), listado na parte superior da etiqueta, bem como o número do lote e a data de validade, listados no lado esquerdo do rótulo. Todos os produtos afetados tinham 90 comprimidos cada.
O produto recordado de 10 mg possui um NDC de 0071-053-23, um número de dr9639 e uma data de validade de 31 de março de 2023. Os produtos recordados com 20 mg têm um NDC de 0071-0532-23, números de lote de DX8682 e DG1188 e datas de validade de 31 de março de 2023 e 31 de maio de 2022, respectivamente. Os produtos recordados com 40 mg têm um NDC de 0071-0535-23. Os produtos do número do lote DX6031 têm uma data de validade de 31 de março de 2023, enquanto os produtos do número do lote CK6260 têm uma data de validade de 31 de maio de 2022.
Os lotes de produto recordados foram distribuídos a atacadistas e distribuidores em todo o U.S. e Porto Rico entre dez. 2019 e abril de 2022, disse o FDA.
Se você tiver um dos produtos afetados, entre em contato com o seu profissional de saúde.

No anúncio da FDA, a Pfizer afirmou que o perfil de benefício/risco da Accupril "permanece positivo com base nos dados atualmente disponíveis" e não houve relatos de eventos adversos relacionados ao recall até o momento. E embora a ingestão de nitrosaminas a longo prazo possa estar associada ao aumento do risco de câncer, "não há risco imediato para os pacientes que tomam este medicamento."
No entanto, se você tiver esse medicamento lembrado, é aconselhável entrar em contato com seus médicos ou prestadores de serviços de saúde sobre opções de tratamento alternativas. Para obter informações sobre o retorno do produto e a reembolso, os pacientes também devem entrar em contato com Sedgwick em 888-345-0481 entre 8 a.m. e 5 p.m. Tempo oriental, de segunda a sexta. O FDA também pede que você relate quaisquer reações adversas ou problemas de qualidade ao programa de relatório de eventos adversos MedWatch on -line, ou por correio ou fax regulares.
Atacadistas e distribuições são instruídos a interromper imediatamente a distribuição e quarentena todos os produtos afetados que possam ter. Se os produtos foram distribuídos ainda mais para locais adicionais, as empresas devem notificar os destinatários e "conduzir uma sub-recall."
Relacionado: Se você usar este medicamento comum, ligue para o seu médico agora, alerta a FDA.


