4 medicamentos que os médicos nunca mais prescrevem

Quando você confia sua saúde a um médico, pode pensar que vocês dois são os únicos partidos que fazem chamadas cruciais sobre o seu bem -estar. Mas o segundo seu médico pega um bloco de prescrição, esse círculo de confiança se expande para incluir empresas farmacêuticas e agências regulatórias. Infelizmente, como todos sabemos de recalls de alto nível em que os medicamentos são retirados do mercado, a indústria farmacêutica às vezes comete erros. Embora todos os medicamentos tenham riscos e benefícios, certos produtos provaram ser simplesmente perigosos demais para serem assumidos, causando danos evitáveis e irreversíveis ou até morte.
Enquanto isso, muitos medicamentos com efeitos colaterais graves permanecem no mercado ou retornam após um breve recall. É preciso muito para as drogas serem retiradas das prateleiras permanentemente, mas isso acontece. Continue lendo para descobrir mais de quatro medicamentos que os médicos provavelmente nunca mais prescreverão e para ouvir as histórias surpreendentes de por que eles não são mais prescritos.
Leia o próximo: as principais farmácias estão bloqueando este medicamento diário comum.
1 Vioxx para artrite

Vioxx é um inibidor da COX-2 que já foi comumente usado para tratar a artrite. Mas em 2004, o fabricante da droga, Merck & Co., Se tivesse retido o mercado quando surgiu as notícias de que havia sido vinculado a 88.000 ataques cardíacos entre 1999 e 2003-38.000, dos quais eram fatais. Quando foi retirado do mercado, estima -se que mais de 20 milhões de pacientes tivessem tomado o medicamento. Em 2007, Merck atingiu um 4.Liquidação de 85 bilhões de dólares para resolver milhares de ações judiciais-o maior assentamento de drogas da história, de acordo com a NPR.
"Certamente há uma necessidade de inibidores da COX-2, mas, finalmente, eles estavam sendo comercializados incorretamente por empresas farmacêuticas aos médicos para usar doses mais altas", diz William Soliman, PhD, BCMAS, fundador e CEO do Conselho de Credenciamento para Assuntos Médicos (ACMA) e um executivo farmacêutico que anteriormente trabalhou com a Merck. "Na minha opinião, isso levou a parte do risco cardiovascular", disse Soliman ao Melhor vida.
2 bextra para alívio da dor

Valdecoxib, com a marca como Bextra, é um medicamento anti-inflamatório não esteróidal (AINE) que já foi prescrito como um alívio de dor. No entanto, em 2005, os pesquisadores descobriram que a droga causou complicações cardiovasculares graves e às vezes fatais, como ataque cardíaco e derrame. Raramente, Bextra também foi encontrado para causar duas reações de pele potencialmente fatais conhecidas como síndrome de Stevens-Johnson e necrólise epidérmica tóxica.
Tendo determinado que Bextra não tinha vantagem particular sobre analgésicos semelhantes que não causaram complicações tão graves, o FDA se moveu para interromper seu uso.
3 Belviq para perda de peso

Lorcaserin, marcado como Belviq ou Belviq XR, foi previamente prescrito como um medicamento para perda de peso depois de ser aprovado em 2012. No entanto, em 2020, o FDA instruiu os médicos a parar de prescrever Lorcaserin depois que um estudo revelou uma ligação entre a medicação e o câncer. AE0FCC31AE342FD3A1346EBB1F342FCB
"Estamos tomando essa ação porque acreditamos que os riscos de Lorcaserin superam seus benefícios com base em nossa revisão completa dos resultados de um ensaio clínico randomizado que avalia a segurança", escreveu o FDA em seu anúncio de recall. "Os profissionais de saúde devem parar de prescrever e distribuir lorcaserina aos pacientes. Entre em contato com pacientes atualmente tomando lorcaserina, informe -os sobre o aumento da ocorrência de câncer observado no ensaio clínico e peça que parem de tomar o medicamento. Discuta medicamentos ou estratégias alternativas de perda de peso com seus pacientes, "o órgão regulatório aconselhou.
Para mais notícias de saúde enviadas diretamente para sua caixa de entrada, inscreva -se em nosso boletim informativo diário.
4 Raptiva para psoríase
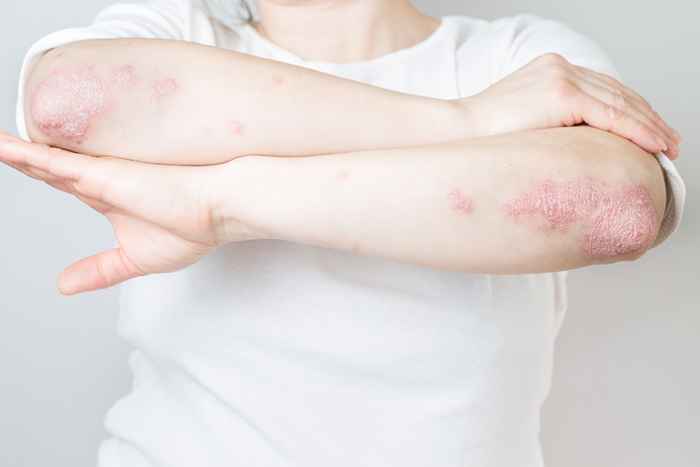
O efalizumab, marcado como Raptiva, foi um medicamento injetável, uma vez por semana, usado para tratar adultos com psoríase de placa moderada a grave. No entanto, em 2009, seu produtor lançou "uma retirada voluntária e faseada do produto do U.S. mercado."
Isso porque os cientistas descobriram que a droga estava ligada à leucoencefalopatia multifocal progressiva (PML), uma doença neurológica rara, mas grave, causada por um vírus que afeta o sistema nervoso central. Em seu aviso de retirada de drogas, o FDA observou que "não há tratamento eficaz conhecido para PML" e, embora seja improvável que qualquer pessoa que leve o Raptiva desenvolva a doença, pode ser fatal naqueles que o contrataram.
A Best Life oferece as informações mais atualizadas dos principais especialistas, novas pesquisas e agências de saúde, mas nosso conteúdo não deve substituir a orientação profissional. Quando se trata da medicação que você está tomando ou de outras perguntas de saúde que você tem, sempre consulte seu médico diretamente.


